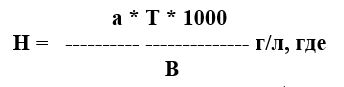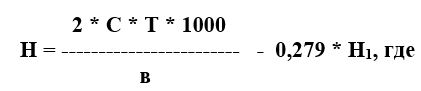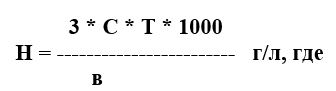Методика анализа раствора для ванн обезжиривания
1.Определение и назначение.
Настоящая инструкция составлена на основании ОСТ 4ГО.054.076 и предназначена для анализа ванн обезжиривания:
1.1 Состав раствора
1.2 Состав раствора
1.3 Состав раствора
1.4 Состав раствора
2. Требования техники безопасности при проведении химических анализов.
2.1Наибольшую опасность представляют:
2.1.2 Химико-термический ожог.
2.2Источники опасности:
2.2.1 Электрооборудование (сушильный шкаф, электроплитка), находящиеся под напряжением.
2.2.2 Концентрированные кислоты и щелочи, используемые при анализе.
2.3. Для обеспечения безопасности работающих необходимо:
2.3.1 Работы с концентрированными растворами кислот, щелочей проводить в вытяжном шкафу.
2.3.2. Использовать индивидуальные средства защиты (халат, очки, перчатки).
2.3.3 Убедиться путём внешнего осмотра в исправности защитного заземления и наружной электропроводки.
2.3.4. При производстве работ соблюдать «Инструкцию по охране труда для лаборантов химической лаборатории участка гальваники и очистных сооружений».
3.Оборудование
3.1 Шкаф вытяжной заводского изготовления
3.2 Посуда мерная лабораторная ГОСТ1770 — 74 Е
3.4 Электроплитка ГОСТ 306 — 76
3.5 Весы лабораторные ГОСТ 24104 — 80
4. Реактивы и материалы
4.1 Барий хлористый 10% ГОСТ 4108 – 72
4.2 Соляная кислота 0,5 Н раствор ГОСТ 3118 – 77
4.3 Фенолфталеин (индикатор) 1% спиртовой раствор ГОСТ 5850 — 72
4.4 Метиловый оранжевый индикатор 0,1% ГОСТ 10816 — 64
4.5 Метиловый красный 0,2% спиртовой раствор ГОСТ 5853-51
4.6 Натрий фтористый ГОСТ 4463-76
4.7 Натрий едкий 0,2 Н раствор ТУ 2642-001-338132-73-97
5. Методы анализа.
5.1 Определение едкого натра.
5.1.1 Сущность метода
Едкий натр в электролите определяется объёмным алкалиметрическим методом после предварительного осаждения углекислого и фосфорнокислого натрия хлористым барием.
5.1.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, прилить 100мл воды, 30мл 10% раствора хлористого бария, 5-6 капель фенолфталеина, перемешать и сразу титровать 0,5 Н раствором соляной кислоты до обесцвечивания раствора.
5.1.3 Расчет:
5.2. Определение натрия углекислого.
5.2.1Сущность метода.
Метод основан на титровании углекислого и фосфорнокислого натрия соляной кислотой в присутствии метилоранжа.
5.2.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, разбавить водой до 50мл, прилить 5-6 капель фенолфталеина и титровать 0,5 Н раствором HCl до обесцвечивания раствора. Затем добавить 2-3 капли метилового оранжевого и продолжать титровать до появления розовой окраски раствора.
5.2.3 Расчет:
5.3. Определение фосфорнокислого натрия.
5.3.1Сущность метода.
Метод основан на титровании общей щёлочности раствором соляной кислоты в присутствии метилового оранжевого. При этом титруют полностью едкий натрий, а трёхзамещённый фосфорнокислый титруется до однозамещённого:
NaOH + HCl = NaCl + H2O
Оттитрованный раствор кипятят для удаления углекислого газа и титруют однозамещённый фосфорнокислый натрий до двухзамещённого раствором едкого натра в присутствии фенолфталеина
5.3.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, разбавить водой до 50мл, прилить 2-3 капли метилового оранжевого и титровать 0,5 Н раствором соляной кислоты до появления розовой окраски раствора. Затем раствор кипятят 5 мин. (для удаления углекислого газа), охладить, прилить несколько капель фенолфталеина и титровать 0,2 Н раствором едкого натра до появления розовой окраски.
5.3.3 Расчет:
5.4. Определение жидкого стекла.
5.4.1Сущность метода.
Метод основан на взаимодействии кремниевой кислоты с фтористым натрием. При этом выделяется эквивалентное жидкому стеклу количество щёлочи, которое оттитровывается раствором соляной кислоты в присутствии метилового красного.
5.4.2 Ход анализа
10мл электролита поместить в коническую колбу ёмкостью 250мл, прибавить 30мл воды, 2-3 капли метилового красного и титровать соляной кислотой до появления розовой окраски. Затем добавить 1-3г кристаллического натрия фтористого, 1-2 капли метилового красного, перемешать и титровать соляной кислотой до исчезновения желтой окраски раствора. Титрование заканчивают, когда последние капли придают раствору бледнорозовое постоянное окрашивание.
Обезжиривание поверхности.
Качество гальванических покрытий в значительной степени зависит от предварительной обработки, в частности, от обезжиривания поверхности деталей (см. «Причины нарушения качества гальванических покрытий»).
Гальванические покрытия практически повторяют микрорельеф поверхности, поэтому декоративность покрытий и коррозионная стойкость могут быть достигнуты только при тщательном обезжиривании поверхности.
Характер загрязнений поверхности деталей может быть различным. Термическая окалина, продукты коррозии, сульфидные и окисные пленки удаляются травлением.
Загрязнения в виде жиров, консервационных смазок, остатков полировочных паст, эмульсий, удаляются в процессе обезжиривания поверхности. Способ обезжиривания поверхности от жировых загрязнений определяется их природой. Жиры минерального происхождения (полировочные пасты, смазки, минеральные масла), которые не растворяются в воде, удаляют при обезжиривании поверхности органическими растворителями. Жиры растительного или животного происхождения, которые не растворяются в воде, но взаимодействуют с водными растворами щелочей, удаляют при обезжиривании поверхности растворами солей щелочных металлов, образуя при этом растворимые мыла.
Наиболее широко оптимальные методы обезжиривания рассматриваются в нашем обучающем курсе.
Обезжиривание поверхности в органических растворителях.
Органические растворители очень токсичны. Применять их можно только при наличии специального оборудования и соблюдения правил техники безопасности (см. «Безопасная гальваника»). Наиболее широко в настоящее время для обезжиривания поверхности используются негорючие растворители: трихлорэтилен, тетрахлорэтилен, четыреххлористый углерод и фреон.
Установка для обезжиривания деталей
В трихлорэтилене можно проводить обезжиривание поверхности большинства металлов: стали, меди, никеля и их сплавов. Из-за большой реакционной способности не допускается обезжиривание деталей, смоченных водой, так как при этом трихлорэтилен разлагается с образованием паров соляной кислоты, что вызывает коррозию аппаратуры.
В трихлорэтилене не допускается обезжиривание деталей из алюминия и титана, поскольку при этом раствор нагревается и происходит разложение с выделением ядовитых соединений.
Наиболее универсальным являются фторсодержащие углеводороды (фреон Ф-113). Обезжиривание поверхности проводится на оборудовании, исключающем попадание паров в атмосферу.
Процесс обезжиривания поверхности деталей в органических растворителях не обеспечивает полного удаления загрязнений, поэтому после просушки детали поступают на химическое или электрохимическое обезжиривание.
Химическое обезжиривание поверхности деталей.
Химическое обезжиривание заключается в том, что под воздействием щелочи жиры омыляются и переходят в раствор, а минеральные масла в присутствии специальных поверхностно-активных веществ образуют эмульсию.
Растворы для химического обезжиривания поверхности содержат щелочи, фосфаты, силикаты, различные ПАВ (синтанол, ДС-10, синтамид-5 и др.). По степени щелочности они разделяются на три группы: сильнощелочные, среднещелочные и слабощелочные.
Для обезжиривания поверхности деталей из алюминия, цинка и олова применяют слабоконцентрированные щелочные растворы, сильно концентрированные – для обезжиривания поверхности стальных деталей.
Состав раствора для обезжиривания поверхности легких сплавов содержит, г/л:
Гидроокись натрия 8 – 12
Натрий фосфорнокислый 20 – 50
Стекло натриевое жидкое 25 – 30
Температура 40 – 70ºС, время 3 – 10 минут
Универсальный раствор химического обезжиривания поверхности для любых металлов содержит 20 – 30 г/л моющего средства «Лабомид» или «Деталин» или «Импульс», при температуре 60 – 80°С время обработки 3 – 10минут.
В качестве замены процесса обезжиривания поверхности в органических растворителях применяют химическое обезжиривание поверхности в моющих средствах КМ-1, лабомид-203, МЛ-52 и др., в состав которых входят триполифосфаты, синтанол ДТ-7, кальцинированная сода, акрилсульфаты.
Для обезжиривания поверхности стали подходят моющие средства: КМ-1, КМ-2, КМ-3, лабомид-203, МЛ-52 и др. в количестве 15 – 30 г/л, при температуре 50 – 70ºС время обработки 5 – 20 минут.
Для обезжиривания поверхности меди, серебра, титана, никеля, инвара и цинка наиболее оптимальны моющие средства: МЛ-51, КМЭ-1, ОС-1, КМ-2, МЛ-52, лабомид-203 и др. концентрацией 60 – 80 г/л, время обработки 3 – 15 минут при температуре 60 – 80ºС.
Обезжиривание поверхности алюминиевых сплавов проводят в моющих средствах: КМ-2, КМ-5, КМЭ-1, МЛ-52, МС-8, лабомид-203 с концентрацией 10 – 20 г/л. Температура 50 – 60ºС, время 5 – 10 минут.
Электрохимическое обезжиривание.
Электрохимическое обезжиривание поверхности металлов является эффективным способом очистки от тонких жировых пленок, которые трудно удалить другим способом. При воздействии тока ионы водорода восстанавливаются на катоде в виде пузырьков, облегчающих отрыв капель масла при обезжиривании от поверхности деталей. Однако при этом может происходить наводораживание поверхности стальных деталей, вследствие чего тонкостенные изделия и пружины могут охрупчиваться, поэтому чаще применяют комбинированный способ обезжиривания поверхности: 5 – 8 минут на катоде, 1 – 2 минуты на аноде.
Электрохимическое обезжиривание поверхности деталей из меди, цинка, алюминия и их сплавов осуществляют только на катоде. Скорость очистки при электрохимическом обезжиривании поверхности деталей гораздо выше, чем при химическом обезжиривании поверхности, качество лучше. Недостаток – низкая рассеивающая способность электролита, поэтому процесс обезжиривания поверхности сложных деталей проводить весьма затруднительно.
В целях безопасности необходимо в процессе электрохимического обезжиривания удалять с поверхности электролита пену, так как в ней может содержаться гремучий газ (смесь водорода и кислорода) и не следует добавлять большое количество эмульгаторов и ПАВ. Увеличение температуры ускоряет процесс обезжиривания поверхности, повышает электропроводность раствора, что позволяет увеличить плотность тока.
Методика анализа раствора для ванн обезжиривания
1.Определение и назначение.
Настоящая инструкция составлена на основании ОСТ 4ГО.054.076 и предназначена для анализа ванн обезжиривания:
1.1 Состав раствора
1.2 Состав раствора
1.3 Состав раствора
1.4 Состав раствора
2. Требования техники безопасности при проведении химических анализов.
2.1Наибольшую опасность представляют:
2.1.2 Химико-термический ожог.
2.2Источники опасности:
2.2.1 Электрооборудование (сушильный шкаф, электроплитка), находящиеся под напряжением.
2.2.2 Концентрированные кислоты и щелочи, используемые при анализе.
2.3. Для обеспечения безопасности работающих необходимо:
2.3.1 Работы с концентрированными растворами кислот, щелочей проводить в вытяжном шкафу.
2.3.2. Использовать индивидуальные средства защиты (халат, очки, перчатки).
2.3.3 Убедиться путём внешнего осмотра в исправности защитного заземления и наружной электропроводки.
2.3.4. При производстве работ соблюдать «Инструкцию по охране труда для лаборантов химической лаборатории участка гальваники и очистных сооружений».
3.Оборудование
3.1 Шкаф вытяжной заводского изготовления
3.2 Посуда мерная лабораторная ГОСТ1770 — 74 Е
3.4 Электроплитка ГОСТ 306 — 76
3.5 Весы лабораторные ГОСТ 24104 — 80
4. Реактивы и материалы
4.1 Барий хлористый 10% ГОСТ 4108 – 72
4.2 Соляная кислота 0,5 Н раствор ГОСТ 3118 – 77
4.3 Фенолфталеин (индикатор) 1% спиртовой раствор ГОСТ 5850 — 72
4.4 Метиловый оранжевый индикатор 0,1% ГОСТ 10816 — 64
4.5 Метиловый красный 0,2% спиртовой раствор ГОСТ 5853-51
4.6 Натрий фтористый ГОСТ 4463-76
4.7 Натрий едкий 0,2 Н раствор ТУ 2642-001-338132-73-97
5. Методы анализа.
5.1 Определение едкого натра.
5.1.1 Сущность метода
Едкий натр в электролите определяется объёмным алкалиметрическим методом после предварительного осаждения углекислого и фосфорнокислого натрия хлористым барием.
5.1.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, прилить 100мл воды, 30мл 10% раствора хлористого бария, 5-6 капель фенолфталеина, перемешать и сразу титровать 0,5 Н раствором соляной кислоты до обесцвечивания раствора.
5.1.3 Расчет:
5.2. Определение натрия углекислого.
5.2.1Сущность метода.
Метод основан на титровании углекислого и фосфорнокислого натрия соляной кислотой в присутствии метилоранжа.
5.2.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, разбавить водой до 50мл, прилить 5-6 капель фенолфталеина и титровать 0,5 Н раствором HCl до обесцвечивания раствора. Затем добавить 2-3 капли метилового оранжевого и продолжать титровать до появления розовой окраски раствора.
5.2.3 Расчет:
5.3. Определение фосфорнокислого натрия.
5.3.1Сущность метода.
Метод основан на титровании общей щёлочности раствором соляной кислоты в присутствии метилового оранжевого. При этом титруют полностью едкий натрий, а трёхзамещённый фосфорнокислый титруется до однозамещённого:
NaOH + HCl = NaCl + H2O
Оттитрованный раствор кипятят для удаления углекислого газа и титруют однозамещённый фосфорнокислый натрий до двухзамещённого раствором едкого натра в присутствии фенолфталеина
5.3.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, разбавить водой до 50мл, прилить 2-3 капли метилового оранжевого и титровать 0,5 Н раствором соляной кислоты до появления розовой окраски раствора. Затем раствор кипятят 5 мин. (для удаления углекислого газа), охладить, прилить несколько капель фенолфталеина и титровать 0,2 Н раствором едкого натра до появления розовой окраски.
5.3.3 Расчет:
5.4. Определение жидкого стекла.
5.4.1Сущность метода.
Метод основан на взаимодействии кремниевой кислоты с фтористым натрием. При этом выделяется эквивалентное жидкому стеклу количество щёлочи, которое оттитровывается раствором соляной кислоты в присутствии метилового красного.
5.4.2 Ход анализа
10мл электролита поместить в коническую колбу ёмкостью 250мл, прибавить 30мл воды, 2-3 капли метилового красного и титровать соляной кислотой до появления розовой окраски. Затем добавить 1-3г кристаллического натрия фтористого, 1-2 капли метилового красного, перемешать и титровать соляной кислотой до исчезновения желтой окраски раствора. Титрование заканчивают, когда последние капли придают раствору бледнорозовое постоянное окрашивание.
Способ количественного определения фосфатов, карбонатов и гидроксида натрия
ВЕДОМСТВО СССР (ГОспАтент сссР)
ОПИСАНИЕ ИЗОБРЕТЕНИЯ (я)5 G 01 N 31/16 д,,g y
° ь лити кисл венн фос или обез крыт прои прав тато опре ната визу эакл ниис фтал хлор карб (21) (22) (46) (71) тит (72) с,м, (56) роль стро (54)
ГИД (57) Т0РСКОМУ СВИДЕТЕЛЬСТВУ
7,02.93, Бюл. ¹ 5 ижегородский политехнический инсА.П. Арбатский, Л.Г; Рыбакова и
Хвощева ячеславов П.M.. Шмелева Н.М. Контэлектролитов и покрытий. Л.: Машиноние, 1985, с. 97.
ПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕНИЯ ФОСФАТОВ, КАРБОНАТОВ И
ОКСИДА НАТРИЯ спольэование: в области аналитичехимии, для кислотно-основного раззобретение относится к области аначеской химии, а именно к способу тно-основного раздельного количестго определения компонентов смеси атов, карбонатов и гидроксида натрия уры в электролитах ванн химического иривания перед гальваническими rioями, предназначенному для контроля водства и позволяющему повысить льность и воспроизводимость резульаналиэа, качестве прототипа выбран способ еления гидроксида, фосфата и карбонатрия методом кислотно-основного льного индикаторного титрования. Он чается в последовательном титроваляной кислотой с индикатором фенолином (титруется гидроксид натрия до да натрия, фосфат до гидрофосфата и нат до гидрокарбоната) и метиловым
2 дел ьного кол ичествен ного определения смеси фосфатов, карбонатов и гидроксида натрия в электролитах ванн химического или электрохимического обезжиривания перед гальваническими покрытиями. Сущность способа заключается в том, что кислотно-основное титрование проводят с потенциометрической индикацией конечных точек путем титрования пикриновой кислотой до первых двух скачков в ацетонводной среде, а для получения третьего скачка в раствор вводят диметилформамид в количестве; обеспечивающем соотношение ацетона, воды и диметилформамида
1:(1 — 1.5):(4 — 5) по объему. 1 табл.
ЪФ оранжевым (гидрофосфат до дигидрофосфата и гидрокарбонат до угольной кислоты).
Далее раствор кипятят до удаления СОэ и титруют раствором гидроксида натрия до К ) изменения окраски раствора за счет фенол-. р фталеина.
1793369 исключает применение этого способа для контроля электролитов ванн подготовки алюминия и его сплавов перед гальваническими покрытиями.
Цель изобретения — повышение правильности и воспроизводимости определения фосфата, карбоната и гидроксида натрия или буры при совместном присутствии в электролитах ванн химического обезжиривания. Цель достигается тем, что в «0 способе количественного определения фосфатов, карбонатов и гидроксида натрия кислотно-основное титрование проводят с потенциометрической индикацией конечных точек, причем в качестве титранта ис- 15 пользуют ацетон-водный раствор пикриновой кислоты, Титрование до первых двух скачков осуществляют в ацетон-водной среде, а для получения третьего скачка в раствор вводят диметилформамид до соот- 20 ношения ацетона, воды и диметилформамида, равного 1:(1 — 1,5):(4-5) по обьему.
При титровании в ацетон-водной среде на кривой имеются два скачка. Первый отвечает окончанию взаимодействия с пикри- 25 новой кислотой фосфата до гидрофосфата, карбонаты до гидрокарбоната, гидроксида натрия до хлорида или буры до борной кислоты. Второй — переходу гидрофосфата до дигидрофосфата, а гидрокарбоната до 30 угольной кислоты. Ацетон вводят для создания лучших условий дпя раздельного титрования компонентов (более резко выражен первый скачок, что способствует повышению правильности и воспроизводимости ре- 35 зультатов), так как возрастает протяженность шкалы кислотности растворителя и компоненты дифференцируются по ступеням диссоциации. Эффект возрастания первого скачка наблюдается при со- «0 отношении воды и ацетона меньше 1,5:1 по объему. При соотношении меньше 1;1 растворимость фосфатов, карбонатов и буры понижается и образуются осадки, что приводит к невозможности проведения титра- 45 ванна, Появление третьего скачка возможно, если фосфорная кислота по первой ст;пени диссоциации и кислота-титрант имеют разницу в константах диссоциации не меньше чем на три-четыре порядка. Это 50 условие реализуется, если в качестве титранта используется пикриновая кислота, а в раствор добавляется диметилформамид.
Соотношение растворителей после добавления диметилформамида должно составлять; 55 ацетон: вода: диметилформамид 1;(1-1,5):(45). При меньшем относительном содержании диметилформамида не набл1одается достаточной разйицы в константах диссоциации пикриновой кислоты и фосфорной кислоты по первой ступени и третий скачок на кривой титрования выражен нечетко. Большее содержание диметилформамида приводит к его необоснованному расходу и к экспериментальным трудностям, связанным со слишком большим объемом раствора в электролитической ячейке для титрования.
Способ осуществляют следующим образом. В ячейку для потенциометрического титрования с помощью пипетки отбирают 5 см испытуемого раствора и добавляют последовательно с помощью мерного цилиндра 10-20 см дистиллированной воды и 15 з см ацетона. Ячейку помещают на магнитную мешалку и погружают в. раствор стеклянный и хлоридсеребряный насыщенный непроточный эаектроды. Титрование осуществляют, прибавляя 0,15 моль/дм расз твора пикриновой кислоты в ацетон-водном растворителе (1,5-2);1 по обьему. рН раствора измеря1от с помощью универсального иономера ЭВ-74 или аналогичного рН-метра. Титрование осуществляют до получения двух скачков на кривой титрования, затем добавляют в ячейку 60 — 75 см диметилформамида и продолжают титрование до получения третьего скачка, При этом соблюдается соотношение сорастворителей: ацетон: вода: диметилформамид, равное 1:(1-1,5):(4 — 5), Количественное содер>кание компонентов в испытуемом растворе (Х, г/дм ) рассчитывают по формулам:
XNa3pOq (V3 V2) С lrNa3POq/V;
XNa2C03 = (2Ч2 — Ч1 — ЧЗ) С lVlrNa2CO31Ч;
X»йаОН = 2(V2 Ч1) С MrNaOH/V
XNa2BqOy = pe Ч1) С MrNa2Bq07 Ч °
«вЂ” при титровании смеси фосфата, карбоната и гидроксида натрия;
«» — при титровании смеси фосфата, карбоната натрия и буры;
V1, Ч2, Чз- обьемы раствора пикриновой кислоты, соответствующие первому, второму и третьему скачкам на кривой титрования, см;
С вЂ” концентрация титранта — пикриновой кислоты, моль/дмз;
V — обьем испытуемого раствора, взятый для анализа (5 см ).
Изобретение иллюстрируется следующими примерами определения компонентов электролитов ванн химического обезжиривания перед гальваническими покрытиями по предлагаемому способу и по известному способу, Содержание компонентов в растворе отвечало ГОСТ 9.305-84
«Покрытия металлические и неметаллические органические», Пример 1. Титрование смеси гидрокс да натрия, карбоната натрия и тринатри фосфата известного состава.
B стакан вместимостью 150 см отбирают 5 см испытуемого раствора известного со тава, добавляют 15 см дистиллированно воды и 15 см ацетона. Стакан помещают на магнитную мешалку, погружают в ра твор стеклянный и хлоридсеребряный эл ктроды. подсоединенные к универсально у иономеру ЭВ-74, Титрование осуществл ют0,15моль/дм растворомпикриновой ки лоты в водно-ацетоновом растворителе с с отношением воды и ацетона 1:2 по объем, Титрант добавляют иэ бюретки порциям по 0,5 см, а в области скачков— з по циями по 0,2 см (для более точного уста овления конечных точек титрования)., По ле получения второго скачка, когда рН ра вора достигает 3,5, в стакан добавляют
70 м диметилформамида (рН раствора при з это возрастает до 5,7) и продолжают титро ание пикриновой кислотой до завершени третьего скачка на кривой титрования, Ко ечные точки на кривой титрования определяют графическим методом, проводя касат льные к трем участкам: до скачка, в пр делах скачка и после скачка. Середины сре них участков определяют койечные точки итрования. Соотношение ацетона, воды и диметилформамида составляет 1;1,2:4,5 по )бъему.
Результаты определения компонентов данной смеси по предлагаемому способу и изв стному способу приведены в таблице.
Пример 2. Титрование пробы производ твенного электролита ванны химическо о обезжиривания.
Для исследования отбирают 5 см произв дственного электролита, содержащего гид оксид натрия, карбонат натрия и тринат ийфосфат. Титрование осуществляют, как казано в примере 1. Соотношение ацетон, воды и диметилформамида то же, что в и имере 1, Параллельно осуществляют тит ование по известному способу.
Результаты определения приведены в таблице.
По данным таблицы видно, что при титров нии искусственной смеси по предлагаемому способу найденное содержание компонентов близко к взятому. По известном способу найденное содержание ком понентов отличается от взятого: для гид оксида натрия и тринатрийфосфата завы ено, для карбоната натрия — занижено, При титровании производственной смеси эта азница возрастает.
Пример 3. Титрование смеси гидроксида натрия, карбоната натрия и тринатрийфосфата при избыточном содержании ацетона.
Для исследования отбирают 5 см испытуемого раствора с составом компонентов, как в примере 1. Добавляют 10 см воды и приливают с помощью цилиндра ацетон.
При добавлении 17 см ацетона начинает з интенсивно выпадать осадок солей. Соотношение ацетона и воды составляет 1;0,9. Ввиду выпадения осадка титрование неприменимо.
Таким образом, при избыточном содержании ацетона титрование становится невозможным, Пример 4, Титрование смеси гидроксида натрия, карбоната натрия и тринатрийфосфата при недостаточном
20 содержании ацетона и диметилформамида.
Для исследования отбирают 5 см испытуемого раствора известного состава. добавляют 20 см дистиллированной воды и 15 з см ацетона. Проводят титрование. как указ
25 зано в примеое 1. добавляя после второго скачка 50 см диметилформамида. Растворитель отвечает отношению ацетона, воды и диметилформамида 1:1,7:3,3.
На кривой титрования наблюдается
30 уменьшение первого и особенно третьего скачков. В пределах добавленного титранта й1% от точки эквивалентности первый скачок уменьшается от 0,55 до 0,45 ед. рН, а третий — от 0,2 до 0,1 ед. рН. Третья конеч35 ная точка при этом устанавливается ненадежно, что приводит к.значительному ухудшению результатов. Уменьшение третьего скачка связано со снижением относительногоо содержания диметилформамида
40 по сравнению с водой, что сокращает протяженность шкалы кислотности растворителя и усиливает обратимость реакции взаимодействия пикриновой кислоты с дигидрофосфатом натрия. Результаты опреде45 лений приседены в таблице. Так как в примерах 3 и 4 соотношение растворителей не отвечало предложенному способу, сопоставление с результатами известного способа не проводилось.
Пример 5. Титрование смеси карбоната натрия. тринатрийфосфата и буры известного состава.
Для исследования отбирают5см испы55 туемого раствора, отвечающего электролиту ванн подготовки алюминия и его сплавов под гальванические покрытия, добавляют
20 см дистиллированной воды, 15 см ацез тона и осуществляют титрование, как в примеое 1, добавляя после второго скачка 75 см диметилформамида. Соотношение аце1793369
Результаты определения компонентов ванн обезжиривания, n=10, Р=0,95